請重點關注《2020年8月我國新注冊臨床的生物創新藥》的部分,其它如《化工合成藥品》部分可以略過。
2020年8月我國藥審中心共計受理961個受理號,同比增加17.9%,相比去年同期增加39.9%。其中化藥占比82%,生物制品占比15%,中藥占比3%。
2020年1-8月我國藥審中心藥品受理情況
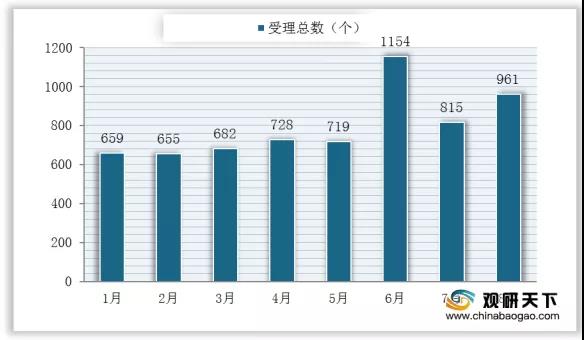
數據來源:國家藥品監督管理局藥品審評中心
2020年8月我國各藥品類型受理情況
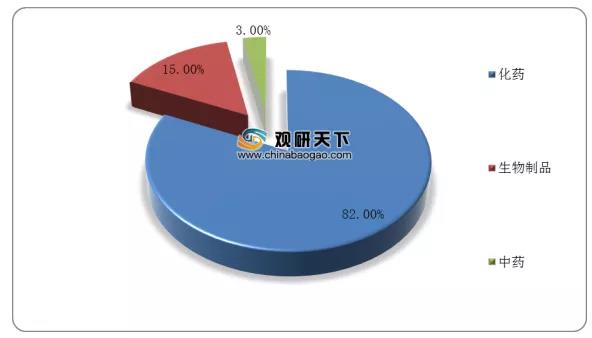
數據來源:國家藥品監督管理局藥品審評中心
一、從各藥品受理情況來看
1、化藥受理情況
2020年8月化藥受理總數為790個,其中補充申請高達590個;化藥1類創新藥新申報共計73個受理號,共計23個品種,涉及23個企業,國產創新藥共計新申報20個品種。
2020年8月我國化藥各申請類型受理情況
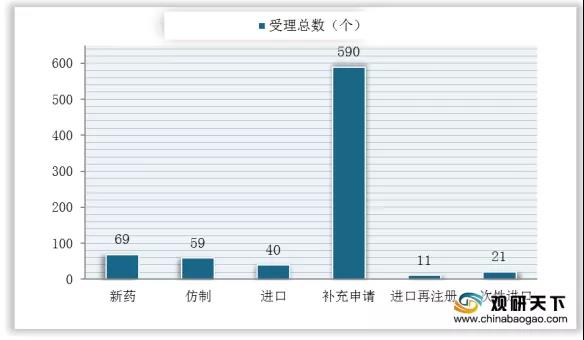
數據來源:國家藥品監督管理局藥品審評中心
2020年8月我國化藥各注冊分類受理情況
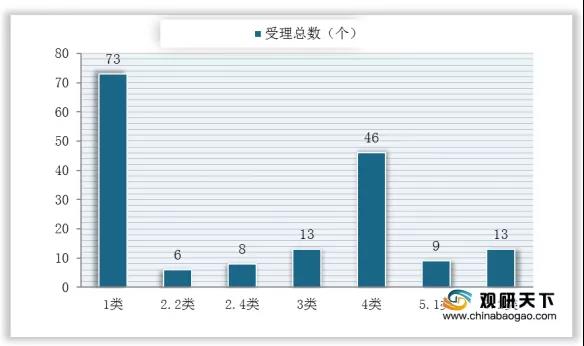
數據來源:國家藥品監督管理局藥品審評中心
其中,明慧醫藥、凌科藥業、蘇州新旭、山東百極地長制藥、上海潤石醫藥、深圳金瑞基業、北京愛泰浦生物等7家企業為首次申報藥品。
2020年8月我國新注冊臨床的化藥創新藥
|
類型 |
藥品名稱 |
企業名稱 |
適應癥 |
|
國產 |
APG-2575片 |
蘇州亞盛 |
復發/難治慢性淋巴細胞白血病(r/rCLL)或小淋巴細胞淋巴瘤 (r/rSLL) |
|
HW130注射用濃溶液 |
深圳海王 |
抗腫瘤 |
|
|
PZH2109膠囊 |
片仔癀 |
非酒精性脂肪性肝炎(NASH) |
|
|
MHO48軟膠囊 |
明慧醫藥 |
|
|
|
LNKO1001膠囊 |
凌科藥業 |
|
|
|
TDIO1片 |
北京泰德 |
肺纖維化、非酒精性脂肪肝炎 |
|
|
sCo245片 |
石家莊智康弘仁 |
|
|
|
RS1805片 |
瑞石生物 |
|
|
|
ASC40片 |
歌禮生物 |
非酒精性脂肪性肝炎(NASH) |
|
|
18F-APN-1607注射液 |
蘇州新旭 |
Tau蛋白正電子發射計算機斷層顯像(PET)示蹤劑 |
|
|
馬來酸博格列汀片 |
山東百極地長 |
|
|
|
ABSKO21膠囊 |
上海和譽生物 |
抗腫瘤 |
|
|
TSL-1806膠囊 |
江蘇天士力帝益 |
|
|
|
TT-00920片 |
南京藥捷安康 |
|
|
|
SYHA1813口服液 |
上海潤石醫藥 |
|
|
|
注射用HY0721 |
蘇州滬云新藥 |
|
|
|
JRF103片 |
深圳金瑞基業 |
|
|
|
注射用ATAP-M8 |
北京愛泰浦生物 |
抗腫瘤 |
|
|
TQB3720片 |
正大天晴 |
|
|
|
HNC664膠囊 |
廣州市恒諾康 |
|
|
|
進口 |
SAR442168 |
賽諾菲 |
復發型多發性硬化癥(RMS) |
|
AMG 650 |
百濟神州 |
|
|
|
Infigratinib膠囊 |
上海聯拓生物 |
膽管癌 |
資料來源:國家藥品監督管理局藥品審評中心
2、生物制品受理情況
2020年8月生物制品共計受理138個,其中主要為治療用生物制品,其受理數高達127個,共計19家企業申報了19個1類生物藥。
2020年8月我國生物制品受理情況
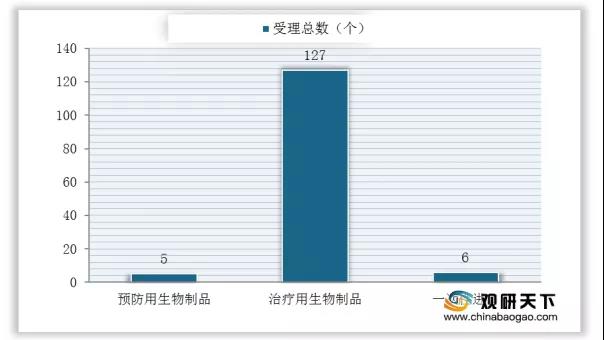
數據來源:國家藥品監督管理局藥品審評中心
2020年8月我國新注冊臨床的生物創新藥
|
受理號 |
藥品名稱 |
企業名稱 |
|
JXSL2000138 |
SAR439459注射用粉針 |
賽諾菲(中國)投資有限公司 |
|
CXSL2000220 |
BAT4706注射液 |
百奧泰生物制藥股份有限公司 |
|
CXSL2000221 |
||
|
CXSL2000224 |
IBI102 |
信達生物制藥(蘇州)有限公司 |
|
JXSL2000141 |
Nirsevimab注射液 |
AstraZeneca AB |
|
CXSL2000229 |
CMG901 |
康諾亞生物醫藥科技(成都)有限公 |
|
CXSL2000230 |
LVGN6051單克隆抗體注射液 |
禮進生物醫藥科技(蘇州)有限公司 |
|
CXSL2000236 |
重組人源化單克隆抗體MIL93注射液 |
北京天廣實生物技術股份有限公司 |
|
CXSL2000237 |
PM8002注射液 |
普米斯生物技術(珠海)有限公司 |
|
CXSL2000239 |
UB-621注射液 |
聯藥(上海)生物科技有限公司 |
|
CXSL2000240 |
枯草桿菌纖溶酶腸溶膠囊 |
武漢真福醫藥股份有限公司 |
|
CXSL2000242 |
IB1323 |
信達生物制藥(蘇州).有限公司 |
|
CXSL2000245 |
注射用GQ1001凍干粉針劑 |
啟德醫藥科技(蘇州)有限公司 |
|
CXSL2000241 |
非小細胞肺腺癌復合抗原致敏的樹突狀細胞所激活的自體T細胞注射液 |
深圳益世康寧生物科技有限公司 |
|
CXSL2000244 |
注射用CN201 |
同潤生物醫藥(上海)有限公司 |
|
CXSL2000247 |
BGB-A1217注射液 |
百濟神州(廣州)生物科技有限公司 |
|
CXSL2000246 |
IAH0968 |
盛禾(中國)生物制藥有限公司 |
|
CXSL2000248 |
RC1012注射液 |
瑞創生物技術有限公司 |
|
CXSL2000252 |
CM313注射液 |
康諾亞生物醫藥科技(成都)有限公 |
|
CXSL2000251 |
注射用SG404 |
中生尚健生物醫藥(杭州)有限公司 |
資料來源:國家藥品監督管理局藥品審評中心
3、中藥受理情況
2020年8月,中藥受理31個受理號,其中25個為補充申請。
二、從各藥品審評完成情況來看
2020年8月,藥審中心完成新報任務審評共計584個,化藥439個,生物制品合計122個,中藥23個。
2020年8月我國各藥品類型審評完成情況
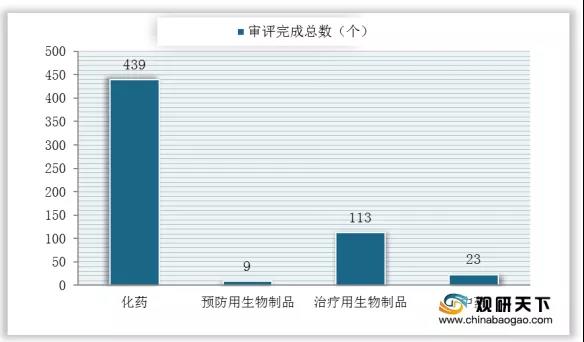
數據來源:國家藥品監督管理局藥品審評中心
1、化藥審評完成情況
2020年8月化藥新報任務審評完成439個受理號,占比75.2%,其中IND審評完成101個受理號,NDA完成10個受理號。
2020年8月化藥新報任務審評完成情況 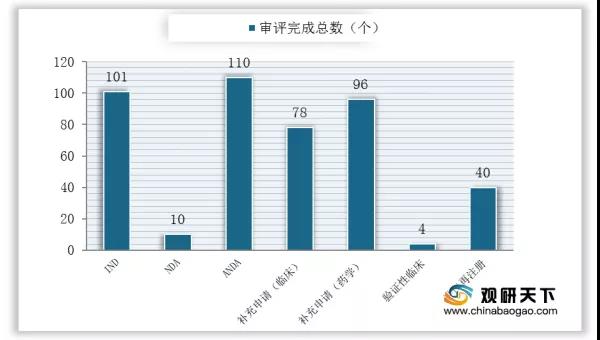
數據來源:國家藥品監督管理局藥品審評中心
從審評時長來看,臨床試驗申請的審評速率依舊保持高效率。其中IND平均審評時長為68天。而NDA、ANDA的審評時長相對較長,并且發補的幾率很高。
2020年8月化藥新報任務審評時長
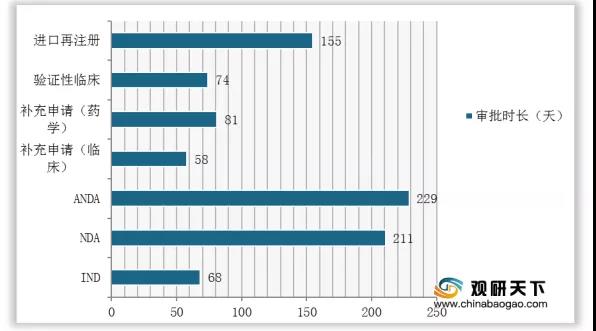
數據來源:國家藥品監督管理局藥品審評中心
2、治療用生物制品審評完成情況
2020年8月,完成治療用生物制品新報任務審評113個受理號。其中,補充申請與臨床占比較大,分別為63個與57個。
2020年8月治療用生物制品新報任務審評完成情況
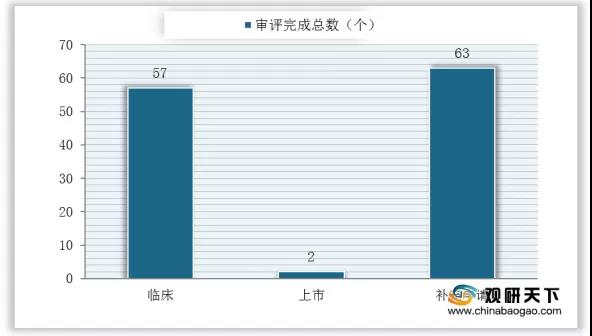
數據來源:國家藥品監督管理局藥品審評中心
3、中藥審評完成情況
2020年8月,共完成中藥審評共計23個,其中有3個中藥品種審評完畢并獲批開展臨床試驗。
2020年8月獲批開展臨床試驗的中藥
|
受理號 |
藥品名稱 |
企業名稱 |
獲批開展臨床適應癥 |
|
CXZL2000008 |
參芪醒腦顆粒 |
北京恒清堂醫藥科技有限公司 |
用于治療輕度老年性癡呆氣虛血滯,瘀濁阻絡之證,見記憶力減退、思維遲鈍、神疲乏力、少氣懶言、頭暈等上述癥狀者。 |
|
CXZL2000009 |
益肺濟生顆粒 |
河南中醫藥大學 |
補益肺腎,止咳平喘。用于慢性阻塞性肺疾病穩定期肺腎氣虛證所致胸悶、喘息、咳嗽、咳痰、氣短、乏力、腰膝酸軟等癥。 |
|
JXZL2000001 |
YIV-906膠囊 |
醫起醫療科技有限公司 |
降低索拉非尼治療乙肝病毒感染相關的晚期肝細胞肝癌時所引起的腸胃副作用及手足綜合征,并增強索拉非尼的抗腫瘤療效。 |
資料來源:國家藥品監督管理局藥品審評中心